pH i jord og matevann er viktige aspekter for en god mateplan. pH har ingen direkte effekt på planten, men påvirker tilgjengeligheten av næringsstoffene for planten direkte. Planten kan også påvirke pH i jorda i området i nærheten av røttene, noe vi vil diskutere senere i denne artikkelen.
For å bedre forstå effekten av pH på dine avlinger, må vi først definere pH. pH-skalaen, standard måleenheten på surhetsgrad, ble utviklet av lederen for Carlsberg-laboratoriets kjemiske avdeling i 1909. Det betyr “hydrogenets kraft” fordi skalaen gir et enkelt og universelt mål på mengden hydrogenioner som finnes i en løsning. Disse ionene påvirker surheten og hvordan løsningen vil reagere kjemisk. pH er definert som den negative logaritmen i konsentrasjonen av hydrogenioner. Det er et resultat av tilstedeværelsen av anioner (negativt ladete næringsstoffer) og kationer (positivt ladete næringsstoffer). pH-skalaen går fra 0 (surt) til 14 (basisk) med ph 7 som nøytralt punkt.
Planten kan påvirke jordlivet i sin rhizosfære
Rhizosfæren er den smale regionen av jord som direkte påvirkes av rotsekresjoner og tilknyttede jordmikroorganismer. Planter responderer på næringsunderskudd ved å endre sin rotmorfologi, rekruttere hjelp fra mikroorganismer og endre det kjemiske miljøet i rhizosfæren. Komponenter i rotsekresjonen hjelper planter med å nå næringsstoffer ved å gjøre dem sure eller endre redoksforholdene inne i rhizosfæren eller chelatere direkte med næringsstoffet. Sekret kan frigjøre næringsstoffer via oppløsning av uløselige mineralfaser eller desorpsjon fra leiremieraler eller organisk materiale, hvor de deretter frigjøres i jorden i oppløsning og kan deretter tas opp av planten. Ved forberedelse av en næringsoppløsning, må en dyrker sørge for at pH i vannet er innenfor en viss rekkevidde. Denne rekkevidden vil helst være der hvor flest næringssotffer tilgjengelige for planten, som er 5,2-6,2. Ved behov kan pH i gjødseloppløsningen justeres ved å legge til syre for å senke pH eller base for å øke den. Men i rhizosfæren, de direkte omgivelsene til de levende røttene, blir ting svært annerledes. Røttene skiller ut mange stoffer som endrer pH i substratet.
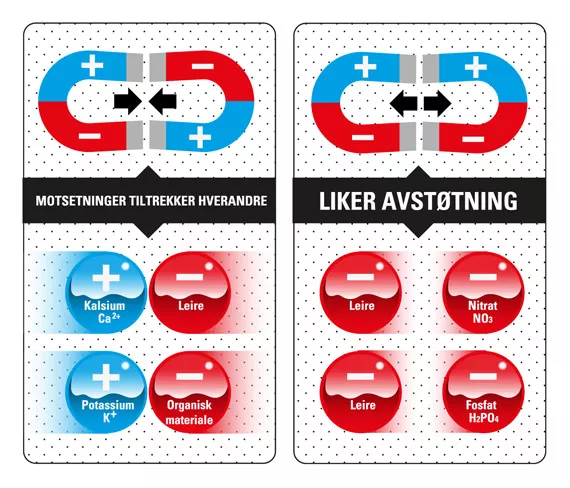
pH i rhizosfæren kan være svært annerledes fra pH som måles i næringsoppløsningen. Hovedårsaken til dette er at planten må holde seg ‘nøytral’. Når de løses opp i vann, presenterer alle næringsstoffer seg som ioner. Disse ionene har alltid en positiv eller negativ ladning. Positivt ladete ioner, som K+, kalles kationer. Negativt ladete ioner, som NO3-, kalles kationer. Noen næringsstoffer kan være til stede i flere former. For eksempel fosfat, som kan oppstå som PO3-, HPO2- og H2Po1-. Kun denne siste formen kan tas opp av røttene. Overflaten av roten er negativt ladet. I denne tilstanden vil de negativt ladete ionene, som H2PO1-, fjernes fra rotoverflaten som to magnet med samme pol. Planter har utviklet flere måter å fasilitere opptak av anioner. For hvert anion planten tar opp, skiller den ut et anion som et hydroksid- (OH-) eller bikarbonation (HCO3-). På samme måte, for hvert kation den tar opp, skiller planten ut et kation som et H+- På denne måten forblir plantens lading balansert. Men en bivirkning av dette er at de utskilte ionene påvirker pHen til rhizosfæren i substratet. Ved å skille ut et kation, senkes pHen nær røttene (de blir surere). Utskillelsen av anioner vil øke pHen nær røttene (de blir mer basiske).
Det er velkjent at nitrogengjødsel har en effekt på pHen nær røttene. Denne innsikten er viktig fordi plantene tar opp så mye nitrogen at effekten kan være betydelig. Men denne effekten oppstår med hvert næringsstoff eller gjødsel. Som dyrker kan du tilsette nitrogen i ulike former. Ammonium (NH4+) har en sur effekt på jorden. Nitrat (NO3-) har en basisk effekt. Man kan lett anta at svaret på dette er å gjødsle med ammoniumnitrat (NH4NO3). Men det er ikke så enkelt. Ammoniumet vil bli tatt opp mye raskere av planten sammenliknet med nitrat, og resultatet vil bli forsurning av jorden. Alle disse reaksjonene må tas hensyn til fordi hvert næringsstoff har sin egen optimale pH-rekkevidde i jorden når det gjelder plantetilgjengelighet. For noen elementer er dette en smal pH-rekkevidde og kun måling av pH i næringsoppløsningen vil ikke fortelle deg hva som faktisk skjer i rhizosfæren.
Sekret
Tidligere var det tydelig at røttene skiller ut mange stoffer for å påvirke jordlivet direkte rundt overflaten av røttene. Disse stoffene kalles ‘sekret’. Hovedsekretene er sukker og organiske syrer. Syrer som sitrisk syre, oksalisk syre og malisk syre er til stede i stor grad i cellefuktigheten i røttene. Disse elementene kan også påvirke pHen i jorden, men hvor sterk denne påvirkningen er, vil variere i hver plante. Hvis syrene skilles ut fra røttene, løses de opp som anioner og vil gjøre jorden nær røttene mer basiske, som andre anioner. Vanligvis vil dette sekretet ha en mindre påvirkning på pHen sammenliknet med den sterke effekten av H+-ionutskillelse. Det som er bemerkelsesverdig, er at ikke hver del av rotsystemet fungerer på samme måte. På tuppen av roten skilles flere H+-ioner ut, mens litt lengre nede, skilles flere anioner ut. Dette har sannsynligvis sammenheng med ulikhetene i opptak av gjødsel.
pH-nivåer påvirker tilgjengeligheten av næringsstoffer og plantenes vekst
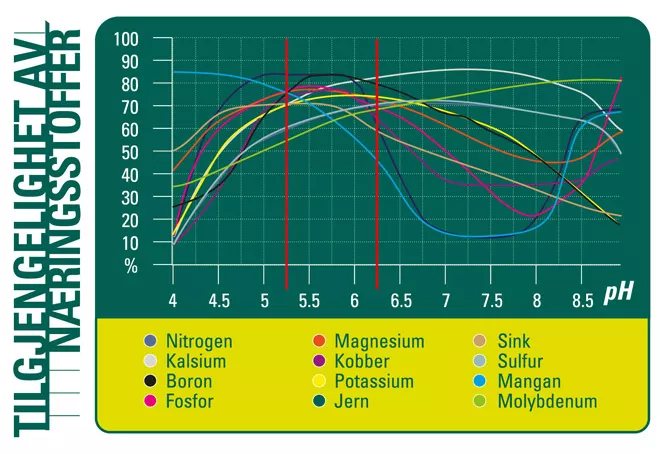
pH-nivået påvirker tilgjengeligheten av næringsstoffer og har derfor også en indirekte effekt på plantenes vekt. pH kan også påvirke absorbpsjon av næringsstoffer i planterøtter. Ikke alle næringsstoffer påvirkes likt, men de fleste næringsstoffer er tilgjengelige for planter i pH-rekkevidden 5,2-6,2 (se figur 4). Før et næringsstoff kan brukes av planten, må det oppløses i jordoppløsningen. De fleste mineraler og næringsstoffer er mer enn løselige, og dermed mer tilgjengelige, i lett sur jord enn i nøytral eller lett basisk jord. I nøytral til lett basisk jord kan noen elementer blir ‘deaktivert’ og ikke lenger være tilgjengelige for planten. Disse elementene inkluderer jern, mangan, kobber, sink og boron. I svært sur jord kan oppløsningsgraden til fosfor, kalsium og magnesium bli redusert. Fosfor er aldri helt løselig i jorden, men er mest tilgjengelig i jord med en pH-rekkevidde på rundt 6,5. Denne verdien varierer mellom ulike substrater. Sur jord (pH 4,0-5,0) kan ha høye konsentrasjoner av løselig aluminium, mangan og jern som kan være giftig for noen planters vekst. Næringsstoffer for sunn plantevekst er delt inn i ulike kategorier: makronæringsstoffer (elementer som trengs i større mengder), som videre deles inn i primære og sekundære næringsstoffer samt mikronæringsstoffer eller sporelementer (elementer som trengs i svært små mengder). De fleste underskudd på sekundære og mikronæringsstoffer kan korrigeres enkelt ved å holde mediet rundt optimalt pH-rekkevidde. Lave pH-verdier (3-5) i kombinasjon med høy temperatur (over 26°C) kan også påvirke vekst av noen soppsykdommer. I svært sur jord kan aktiviteten til bakterier som bryter ned jordorganisk materiale bli påvirket. Dette hindrer organisk materiale i nedbrytning, noe som fører til oppsamling av organisk materiale og mangel på frigjøring av næringsstoffer i jorden, spesielt nitrogen, som blir låst på innsiden av det organiske materialet. Som resultat kan plantenes vekst bli negativt påvirket. I organiske jordsubstrater finnes det fordelaktige sopp kalt mycorrhizae. Disse mikroorganismene foretrekker en lett surt miljø for optimal vekst. Vannets alkalinitet er også en relevant faktor. Hvis vannets alkalinitet er over 200-250ppm CaCO3, bør syre tilsettes for å minimalisere påvirkningen av pHen i vekstmediet.
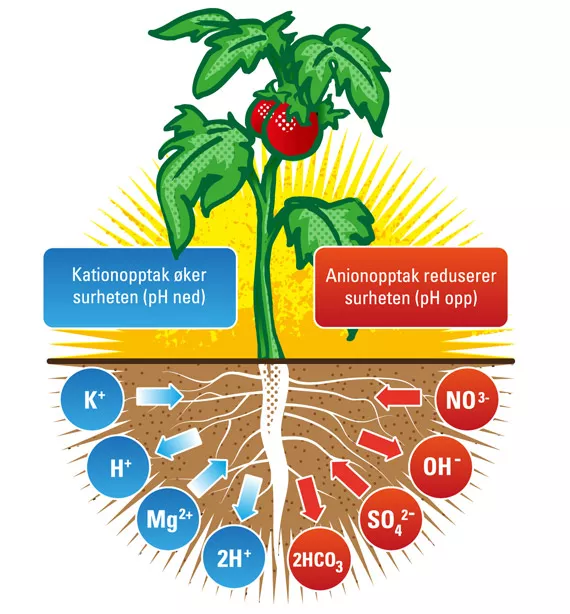
Hvordan og hvorfor pHen ofte endres i hydrofoniske vekstsystemer
Opptaket av anioner (negativt ladete næringsstoffer) og katier (positivt ladete ionere) hos planter kan forårsake betydelige skift i pH i vekstsystemet. Hvis flere kationer absorberes i forhold til anioner, vil pHen synke. Hvis flere anioner absorberes i forhold til kationer, vil pHen øke. Fordi nitrogen (et element som trengs i store mengder for sunn plantevekst) kan tilføres enten som et kation (ammonium - NH1+) eller som et anion (nitrat - NO3-), kan ratioen mellom disse to nitrogenformene i næringsoppløsningen ha en stor effekt på både hastigheten og retningen som pHen endres i over tid. pH-skifte kan oppstå overraskende raskt. De fleste varianter av grønnsaker vokser best i en næringsoppløsning med en pH mellom 5,2 og 6,2 og ved temperaturer mellom 20°C og 22°C.
Når lite lys er tilgjengelig (på overskyede dager eller i innendørs vekstmiljøer), vil planter absorbere mer potassium og fosfor fra næringsoppløsningen, noe som øker surhetsgraden (pHen vil synke). Ved lave lysnivåer senkes transpirasjonshastigheten også, noe som igjen reduserer kalsiumopptaket. I kombinasjon med en lav pH i substratet, kan symptomer på kalsiumunderskudd oppstå. Når det finnes masse intenst lys (på klare soldager), vil plantene ta opp mer nitrogen fra næringsoppløsningen. Som resultat vil surhetsgraden reduseres (pHen øker).
Hva som skjer hvis pHen er for høy eller lav og hvordan du gjenkjenner symptomene
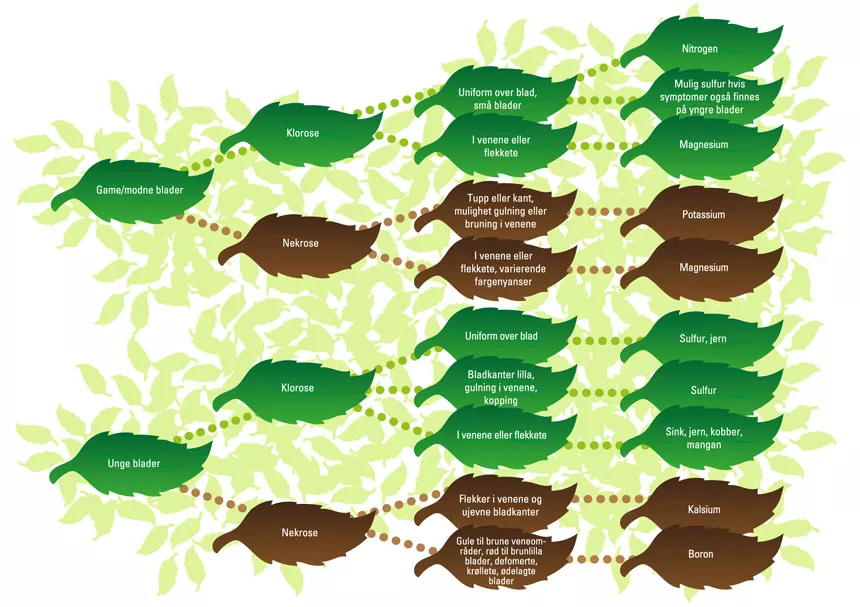
De første symptomene på et underskudd av næringsstoffer vil vises på bladene. Et jernunderskudd (Fe) kan for eksempel oppstå svært raskt. Ved pH-verdier på 7 eller over, vil mindre enn 50% av Fe være tilgjengelig for plantene. Ved pH-verdier på 8,0, vil kun en liten mengde Fe være igjen i oppløsningen på grunn av jernhydroksidpresipirasjon (Fe(OH)3- som etter hvert konvertere til rust). Figur 5 kan brukes som et verktøy for å identifisere underskudd av næringsstoffer i planter. Klorose er gulning eller bleking av grønt plantevev på grunn av tap av klorofyll. Nekrose er død i plantevev og vises som mørk brun misfarging, f.eks. på en del av bladet.
Stedet på planten hvor symptomene oppstår (gamle vs. Unge blader) vil avhenge av mobiliteten til elementet i planten. Elementer med svært lav mobilitet er boron, kalsium, kobber, jern, mangan, molybdenum og sink. Underskudd på disse elementene vil først ses i de yngre bladene. Disse elementene overføres med flyten av sevje til de yngre bladene. De beveger seg ikke rundt inne i planten. Flere mobile elementer er nitrogen, potassium og magnesium. Symptomer på underskudd av disse elementene ses i de eldre bladene på plantene fordi elementene flytter seg fra de eldre bladene til de yngre bladene, som trenger flere næringsstoffer i vekstprosessen.

